Ukupna unutrašnja energija. Velika enciklopedija nafte i gasa
Znamo da se unutrašnja energija tijela može mijenjati na dva načina - vršenjem rada i prijenosom topline. Prilikom primjene prve od ovih metoda unutrašnja energija tijela mijenja se za količinu savršenog rada A, a pri primjeni druge za količinu jednaku količini prenesene topline Q.
Početnu unutrašnju energiju tijela označavamo kroz U 1, a konačnu (nakon što je promijenjena) - kroz U 2. Tada će promjena unutrašnje energije tijela biti jednaka razlici U 2 -U 1. Promjena bilo koje fizičke veličine u fizici se obično označava grčkim slovom A (delta). Stoga možemo napisati:
ΔU - promjena unutrašnje energije
U \u003d U 2 - U 1
Promjena unutrašnje energije može se izraziti i pozitivno i negativno:
1) ako se unutrašnja energija tela povećava, tada je U 2 > U 1 i, prema tome, ΔU > 0;
2) ako se unutrašnja energija tijela smanji, tada je U 2< U 1 и, следовательно, ΔU < 0.
U zavisnosti od toga na koji način (radom na telu ili prenosom toplote) se promenila unutrašnja energija tela, njena promena se može izračunati na dva načina:
ΔU = A - kada se radi (33.1)
ΔU = Q - za prijenos topline (33.2)
Prilikom primjene jednačine (33.1), treba imati na umu da se rad pojavljuje na desnoj strani spoljne sile deluje na telo. Rad tijela A tijela razlikuje se od njega po predznaku:
A tijelo = -A
Količina topline Q također može biti i pozitivna i negativna:
1) ako se unutrašnja energija tela povećava u procesu prenosa toplote, onda Q> O (telo prima količinu toplote);
2) ako se unutrašnja energija tijela smanji u procesu prijenosa topline, onda Q<0 (тело отдает количество теплоты).
U opštem slučaju, unutrašnja energija tela (ili sistema tela) može se promeniti na dva načina odjednom - i radom i prenosom toplote. Zatim se za izračunavanje promjene unutrašnje energije koristi jednačina
ΔU = A + Q (33.3)
Prema ovoj jednačini, promjena unutrašnje energije sistema jednaka je zbiru rada vanjskih sila i količine topline koju primi sistem.
1. Kako se označava unutrašnja energija tijela i promjena unutrašnje energije tijela? 2. U kom slučaju je promjena unutrašnje energije tijela pozitivna, a u kojem negativna? 3. Koji je znak: a) količine toplote koju tijelo primi; b) količinu toplote koju telo daje? Zašto? 4. Napišite formulu koja izračunava promjenu unutrašnje energije tijela tokom prijenosa topline. 5. Napišite formulu koja izračunava promjenu unutrašnje energije tijela kada se na njemu vrši rad. 6. Koja se formula koristi za izračunavanje promjene unutrašnje energije u opštem slučaju?
Glavna karakteristika unutrašnjeg stanja fizičkog sistema je njegova unutrašnja energija.
Unutrašnja energija (U) uključuje energiju haotičnog (toplinskog) kretanja svih mikročestica sistema (molekula, atoma, jona itd.) i energiju interakcije ovih čestica, tj. kinetička, potencijalna itd., osim ukupne energije mirovanja svih čestica.
Svojstva unutrašnje energije
1. U stanju termodinamičke ravnoteže, čestice koje čine makroskopska tijela kreću se tako da je njihova ukupna energija uvijek jednaka unutrašnjoj energiji tijela sa velikom preciznošću.
2. Unutrašnja energija je funkcija stanja fizičkog sistema.
3. Unutrašnja energija fizičkog sistema ne zavisi od putanje njegovog prelaska iz jednog stanja u drugo, već je određena samo vrednostima unutrašnje energije u početnom i konačnom stanju: D U \u003d U 2 -U 1 .
4. Unutrašnju energiju karakteriše svojstvo aditivnosti, tj. jednaka je ukupnoj unutrašnjoj energiji tijela uključenih u sistem.
Napomena: čestice gasa, pored translacionih stepena slobode, imaju i unutrašnje. Na primjer, ako su čestice plina molekule, tada je, osim elektronskog kretanja, moguća i rotacija molekula, kao i vibracije atoma koji čine molekule.
Translatorno kretanje čestica gasa podleže klasičnim zakonima, a njihova unutrašnja kretanja su kvantne prirode. Samo pod određenim uslovima unutrašnji stepeni slobode se mogu smatrati klasičnim.
Da bi se izračunala unutrašnja energija idealnog gasa, koristi se zakon ravnomerne podele energije na klasične stepene slobode. Samo u slučaju idealnog gasa kinetička energija translatorno kretanje čestica. Ako su čestice gasa pojedinačni atomi, onda svaka ima tri translaciona stepena slobode.
Dakle, svaki atom ima prosječnu kinetičku energiju:
< e k > =3 kT/2.
Ako se plin sastoji od N atoma, onda je njegova unutrašnja energija
Ako su i vibracijski stepeni slobode molekula pobuđeni, onda je njihov doprinos unutrašnjoj energiji
| |
(1.27) |
Formula (1.27) uzima u obzir da svako oscilatorno kretanje molekula karakteriše prosečna kinetička i prosečna potencijalna energija, koje su međusobno jednake. Prema tome, prema zakonu ravnomjerne podjele energije na stepene slobode, jedan vibracioni stepen slobode predstavlja prosječnu energiju kT.
Dakle, ako je molekul dvoatomski, onda je ukupan broj njegovih stupnjeva slobodei=6. Tri od njih su progresivna (i brzo =3), dvije rotacijske (i vr =2) i jedan vibracioni (i count =1). Na temperaturama kada su vibracioni stepeni slobode još uvek „zamrznuti“, unutrašnja energija dvoatomskih molekula idealnog gasa
![]() .
.
Ako su vibracijski stupnjevi slobode „odmrznuti“, tada je unutrašnja energija dvoatomskih molekula idealnog plina U = U post + U vr + U count =.
Dakle, unutrašnja energija jednoatomskog idealnog gasa
| U=N < e k >= (3/2)NkT, |
(1.28) |
gdje< e k > = .
Broj molova gasa n=N/N a = m/M, onda
Svako makroskopsko tijelo ima energije zbog svog mikrostanja. Ovo energije pozvao interni(označeno U). Ona je jednaka energiji kretanja i interakcije mikročestica koje čine tijelo. dakle, unutrašnja energija idealan gas sastoji se od kinetičke energije svih njegovih molekula, od njihove interakcije u ovaj slučaj može se zanemariti. Stoga je unutrašnja energija zavisi samo od temperature gasa ( u~T).
Model idealnog plina pretpostavlja da su molekuli na udaljenosti od nekoliko promjera jedan od drugog. Stoga je energija njihove interakcije mnogo manja od energije kretanja i može se zanemariti.
U stvarnim gasovima, tečnostima i čvrstim materijama interakcija mikročestica (atoma, molekula, jona itd.) se ne može zanemariti, jer značajno utiče na njihova svojstva. Stoga, njihova unutrašnja energija sastoji se od kinetičke energije toplotnog kretanja mikročestica i potencijalne energije njihove interakcije. Njihova unutrašnja energija, osim temperature T, zavisiće i od jačine zvuka V, budući da promjena volumena utječe na udaljenost između atoma i molekula, a samim tim i na potencijalnu energiju njihove međusobne interakcije.
Unutrašnja energija je funkcija stanja tijela koje je određeno njegovom temperaturomTi tom V.
Unutrašnja energija jedinstveno određena temperaturomT i volumen tijela V koji karakterizira njegovo stanje:U=U(T, V)
To promeni unutrašnju energiju tijela, potrebno je zapravo promijeniti ili kinetičku energiju toplinskog kretanja mikročestica, ili potencijalnu energiju njihove interakcije (ili oboje). Kao što znate, to se može učiniti na dva načina - prijenosom topline ili kao rezultat rada. U prvom slučaju to se događa zbog prijenosa određene količine topline Q; u drugom - zbog obavljanja posla A.
Na ovaj način, količina toplote i obavljeni rad su mjera promjene unutrašnje energije tijela:
Δ U=Q+A.
Promjena unutrašnje energije nastaje zbog određene količine topline koju tijelo daje ili prima ili zbog obavljanja rada.
Ako se dogodi samo prijenos topline, onda promjena unutrašnja energija nastaje primanjem ili odavanjem određene količine topline: Δ U=Q. Prilikom zagrijavanja ili hlađenja tijela ono je jednako:
Δ U=Q = cm(T 2 - T 1) =cmΔT.
Prilikom topljenja ili kristalizacije čvrstih materija unutrašnja energija promjene zbog promjene potencijalne energije interakcije mikročestica, jer dolazi do strukturnih promjena u strukturi materije. U ovom slučaju, promjena unutrašnje energije jednaka je toplini fuzije (kristalizacije) tijela: Δ U-Q pl \u003dλ m, gdje λ - specifična toplota fuzije (kristalizacije) čvrstog tela.
Isparavanje tekućine ili kondenzacija pare također uzrokuje promjenu unutrašnja energija, što je jednako toplini isparavanja: Δ U=Q p =rm, gdje r- specifična toplota isparavanja (kondenzacije) tečnosti.
Promjena unutrašnja energija tijelo nakon pogubljenja mehanički rad(bez prijenosa topline) numerički je jednak vrijednosti ovog rada: Δ U=A.
Ako dođe do promjene unutrašnje energije kao rezultat prijenosa topline, ondaΔ U=Q=cm(T2 —T1),iliΔ U= Q pl = λ m,iliΔ U=Qn =rm.
Dakle, sa stanovišta molekularne fizike: materijal sa sajta
Unutrašnja energija tela je zbir kinetičke energije toplotnog kretanja atoma, molekula ili drugih čestica od kojih se sastoji i potencijalne energije interakcije između njih; sa termodinamičke tačke gledišta, to je funkcija stanja tela (sistema tela) koje je jedinstveno određeno njegovim makroparametrima - temperaturomTi tom V.
Na ovaj način, unutrašnja energija je energija sistema, koja zavisi od njegovog unutrašnjeg stanja. Sastoji se od energije toplotnog kretanja svih mikročestica sistema (molekula, atoma, jona, elektrona itd.) i energije njihove interakcije. Praktično je nemoguće odrediti punu vrijednost unutrašnje energije, stoga se izračunava promjena unutrašnje energije Δ u, koja nastaje usled prenosa toplote i obavljanja posla.
Unutrašnja energija tijela jednaka je zbiru kinetičke energije toplinskog kretanja i potencijalne energije interakcije njegovih sastavnih mikročestica.
Na ovoj stranici materijal o temama:
Koji makro parametri određuju energiju unutrašnje energije tijela
Odgovorite kako možete promijeniti unutrašnju energiju tijela
Definicije toplotnog kretanja i unutrašnje energije
-
Teme USE kodifikatora Ključne riječi: unutrašnja energija, prijenos topline, vrste prijenosa topline.
Čestice bilo kojeg tijela - atomi ili molekule - vrše haotično neprekidno kretanje (tzv. termičko kretanje ). Dakle, svaka čestica ima neku kinetičku energiju.
Osim toga, čestice materije međusobno djeluju silama električnog privlačenja i odbijanja, kao i nuklearnim silama. Dakle, čitav sistem čestica dato telo takođe ima potencijalnu energiju.
Kinetička energija toplotnog kretanja čestica i potencijalna energija formiraju se njihove zajedničke interakcije nova vrsta energije, koja se ne svodi na mehaničku energiju tijela (tj. kinetičku energiju kretanja tijela kao cjeline i potencijalnu energiju njegove interakcije s drugim tijelima). Ova vrsta energije naziva se unutrašnja energija.
Unutrašnja energija tijela je ukupna kinetička energija toplinskog kretanja njegovih čestica plus potencijalna energija njihove međusobne interakcije.
Unutrašnja energija termodinamičkog sistema je zbir unutrašnjih energija tela uključenih u sistem.
Dakle, unutrašnju energiju tijela formiraju sljedeći pojmovi.
1. Kinetička energija kontinuiranog haotičnog kretanja čestica tijela.
2. Potencijalna energija molekula (atoma), zbog sila međumolekulske interakcije.
3. Energija elektrona u atomima.
4. Intranuklearna energija.Kada najjednostavniji model supstanca - idealan gas - za unutrašnju energiju, možete dobiti eksplicitnu formulu.
Unutrašnja energija jednoatomskog idealnog gasa
Potencijalna energija interakcije između čestica idealnog plina je nula (podsjetimo da u modelu idealnog plina zanemarujemo interakciju čestica na udaljenosti). Stoga se unutrašnja energija monoatomskog idealnog plina svodi na ukupnu kinetičku energiju translacijske (za poliatomski plin također se mora uzeti u obzir rotacija molekula i vibracije atoma unutar molekula) njegovih atoma. Ova energija se može naći množenjem broja atoma gasa sa prosečnom kinetičkom energijom jednog atoma:
Vidimo da je unutrašnja energija idealnog gasa (masa i hemijski sastav koji su nepromijenjeni) je funkcija samo njegove temperature. Za pravi plin, tekući ili čvrsti, unutrašnja energija će također ovisiti o volumenu - na kraju krajeva, kada se volumen promijeni, relativni položaj čestica se mijenja i, kao rezultat, potencijalna energija njihove interakcije.
Statusna funkcija
Najvažnije svojstvo unutrašnje energije je da jeste državna funkcija termodinamički sistem. Naime, unutrašnja energija je jedinstveno određena skupom makroskopskih parametara koji karakterišu sistem i ne zavisi od „praistorije“ sistema, tj. o stanju u kojem je sistem bio prije i kako je konkretno završio u ovom stanju.
Dakle, tokom prelaska sistema iz jednog stanja u drugo, promena njegove unutrašnje energije određena je samo početnim i konačnim stanjem sistema i ne zavisi sa putanje tranzicije od početno stanje do kraja. Ako se sistem vrati u prvobitno stanje, tada je promjena njegove unutrašnje energije nula.
Iskustvo pokazuje da postoje samo dva načina da se promijeni unutrašnja energija tijela:
Izvođenje mehaničkih radova;
prijenos topline.Jednostavno rečeno, čajnik možete zagrijati samo sa dva fundamentalno Različiti putevi: utrljajte ga nečim ili zapalite :-) Razmotrimo ove metode detaljnije.
Promjena unutrašnje energije: obavljanje posla
Ako je posao obavljen gore tijela, unutrašnja energija tijela se povećava.
Na primjer, ekser se nakon udarca čekićem zagrije i malo se deformiše. Ali temperatura je mjera prosječne kinetičke energije čestica tijela. Zagrijavanje eksera ukazuje na povećanje kinetičke energije njegovih čestica: u stvari, čestice se ubrzavaju udarcem čekića i trenjem eksera o dasku.
Deformacija nije ništa drugo do pomicanje čestica jedna u odnosu na drugu; Nakon udarca nokat se deformira kompresijom, njegove se čestice približavaju jedna drugoj, između njih se povećavaju odbojne sile, a to dovodi do povećanja potencijalne energije čestica nokta.
Dakle, povećana je unutrašnja energija nokta. To je bio rezultat rada obavljenog na njemu - rad je obavio čekić i sila trenja na dasci.
Ako je posao obavljen sami tijela, tada se unutrašnja energija tijela smanjuje.
Neka se, na primjer, komprimirani zrak u termoizoliranoj posudi ispod klipa širi i podiže određeno opterećenje, čime se vrši rad (proces u toplinski izoliranoj posudi se naziva adijabatski. Proučavat ćemo adijabatski proces uzimajući u obzir prvi zakon termodinamike). Tokom takvog procesa, vazduh će se hladiti – njegovi molekuli, udarajući u pokretni klip, daju mu deo svoje kinetičke energije. (Na isti način, fudbaler, zaustavljajući nogom brzo leteću loptu, pravi pokret nogom od loptu i gasi njenu brzinu.) Zbog toga se unutrašnja energija vazduha smanjuje.
Zrak, dakle, radi zbog svoje unutrašnje energije: budući da je posuda toplinski izolirana, nema dotoka energije u zrak iz bilo kojeg vanjskog izvora, a zrak može crpiti energiju za obavljanje posla samo iz vlastitih rezervi.
Promjena unutrašnje energije: prijenos topline
Prijenos topline je proces prijenosa unutrašnje energije sa toplijeg tijela na hladnije, a nije povezan s obavljanjem mehaničkog rada.. Prijenos topline može se vršiti ili direktnim kontaktom tijela, ili preko međumedija (pa čak i kroz vakuum). Prijenos topline se također naziva izmjena toplote.
Postoje tri vrste prenosa toplote: provodljivost, konvekcija i toplotno zračenje.
Sada ćemo ih detaljnije pogledati.
Toplotna provodljivost
Ako gvozdenu šipku jednim krajem stavite u vatru, tada je, kao što znamo, ne možete dugo držati u ruci. Ulazak u područje visoke temperature, atomi gvožđa počinju intenzivnije da vibriraju (tj. dobijaju dodatnu kinetičku energiju) i nanose jače udarce svojim susedima.
Kinetička energija susjednih atoma također se povećava, a sada ti atomi daju dodatnu kinetičku energiju svojim susjedima. Dakle, od odjeljka do odjeljka, toplina se postupno širi duž štapa - od kraja stavljenog u vatru do naše ruke. Ovo je toplotna provodljivost (Slika 1) (Slika sa Educationalelectronicsusa.com).

Rice. 1. Toplotna provodljivost
Toplotna provodljivost je prijenos unutrašnje energije sa više zagrijanih dijelova tijela na manje zagrijane zbog toplinskog kretanja i interakcije čestica tijela..
Toplotna provodljivost različitih supstanci je različita. Metali imaju visoku toplotnu provodljivost: srebro, bakar i zlato su najbolji provodnici toplote. Toplotna provodljivost tečnosti je mnogo manja. Plinovi toliko loše provode toplinu da već pripadaju toplinskim izolatorima: zbog velikih razmaka između njih, molekule plina međusobno slabo djeluju. Zato se, na primjer, u prozorima izrađuju dvostruki okviri: sloj zraka sprječava izlazak topline).
Stoga su porozna tijela, kao što su cigla, vuna ili krzno, loši provodnici topline. Sadrže zrak u svojim porama. Nije ni čudo što se kuće od cigle smatraju najtoplijim, a na mrazu se ljudi oblače bunde i jakne sa slojem puha ili sintetičke zimnice.
Ali ako zrak tako slabo provodi toplinu, zašto se onda soba zagrijava od baterije?
To se događa zbog druge vrste prijenosa topline - konvekcije.
Konvekcija
Konvekcija je prijenos unutrašnje energije u tekućinama ili plinovima kao rezultat kruženja strujanja i miješanja tvari.
Zrak u blizini baterije se zagrijava i širi. Sila gravitacije koja djeluje na ovaj zrak ostaje ista, ali se sila uzgona iz okolnog zraka povećava, tako da zagrijani zrak počinje da lebdi prema stropu. Na njegovo mjesto dolazi hladan zrak (isti proces, ali u mnogo većim razmjerima, stalno se dešava u prirodi: tako nastaje vjetar), s kojim se ponavlja isto.
Kao rezultat, uspostavlja se cirkulacija zraka, što služi kao primjer konvekcije - distribucija topline u prostoriji vrši se strujama zraka.
Potpuno analogan proces može se uočiti u tečnosti. Kada stavite kotlić ili lonac sa vodom na šporet, voda se zagreva prvenstveno zbog konvekcije (doprinos toplotne provodljivosti vode je ovde vrlo neznatan).
Konvekcijske struje u zraku i tekućini prikazane su na sl. 2 (slike sa physics.arizona.edu).
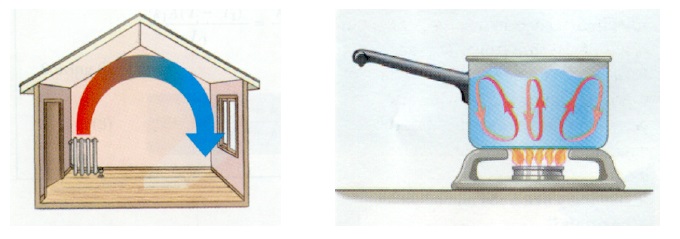
Rice. 2. Konvekcija
U čvrstim tijelima nema konvekcije: sile interakcije čestica su velike, čestice osciliraju u blizini fiksnih prostornih tačaka (čvorova kristalne rešetke) i u takvim uslovima ne mogu se formirati tokovi materije.
Za cirkulaciju konvekcijskih struja prilikom grijanja prostorije potrebno je da se zagrijani zrak bilo je prostora za plutanje. Ako je radijator postavljen ispod stropa, tada neće doći do cirkulacije - topli zrak će ostati ispod stropa. Zbog toga se postavljaju aparati za grijanje na dnu sobe. Iz istog razloga su stavili i čajnik na požara, zbog čega zagrijani slojevi vode, dižući se, ustupaju mjesto hladnijim.
Naprotiv, klima uređaj treba postaviti što je više moguće: tada će ohlađeni vazduh početi da tone, a na njegovo mesto dolazi topliji vazduh. Tiraž će ići na obrnuti smjer u poređenju sa kretanjem tokova prilikom grijanja prostorije.
toplotno zračenje
Kako Zemlja dobija energiju od Sunca? Provođenje toplote i konvekcija su isključeni: dijeli nas 150 miliona kilometara bezzračnog prostora.
Evo treće vrste prenosa toplote - toplotno zračenje. Zračenje se može širiti i u materiji i u vakuumu. Kako nastaje?
Ispostavilo se da je električna magnetsko polje usko povezani jedni s drugima i imaju jedno izuzetno svojstvo. Ako se električno polje mijenja s vremenom, onda ono stvara magnetno polje, koje se, općenito govoreći, također mijenja s vremenom (više o tome će biti riječi u letku o elektromagnetnoj indukciji). Zauzvrat, naizmjenično magnetsko polje stvara naizmjenično električno polje, koje opet stvara naizmjenično magnetsko polje, koje opet stvara naizmjenično električno polje ...
Kao rezultat razvoja ovog procesa, elektromagnetni talas- "zakačeni" jedno za drugo električno i magnetno polje. Kao i zvuk, elektromagnetski valovi imaju brzinu i frekvenciju širenja - u ovom slučaju, to je frekvencija kojom se veličine i smjerovi polja fluktuiraju u valu. vidljivo svjetlo - poseban slučaj elektromagnetnih talasa.
Brzina širenja elektromagnetnih talasa u vakuumu je ogromna: km/s. Dakle, od Zemlje do Mjeseca, svjetlost putuje nešto više od jedne sekunde.
Frekvencijski opseg elektromagnetnih talasa je veoma širok. Više ćemo govoriti o skali elektromagnetnih valova u odgovarajućem listu. Ovdje samo napominjemo da je vidljiva svjetlost mali raspon ove skale. Ispod njega leže frekvencije infracrvenog zračenja, iznad - frekvencije ultraljubičastog zračenja.
Podsjetimo sada da atomi, budući da su općenito električno neutralni, sadrže pozitivno nabijene protone i negativno nabijene elektrone. Ove nabijene čestice, praveći haotično kretanje zajedno s atomima, stvaraju naizmjenična električna polja i na taj način zrače elektromagnetne valove. Ovi talasi se nazivaju toplotno zračenje- kao podsjetnik da je njihov izvor toplotno kretanje čestica materije.
Svako tijelo je izvor toplotnog zračenja. U ovom slučaju, zračenje odnosi dio svoje unutrašnje energije. Susrevši se s atomima drugog tijela, zračenje ih ubrzava svojim oscilirajućim električnim poljem, a unutarnja energija ovog tijela se povećava. Ovako se kupamo na suncu.
Na uobičajenim temperaturama, frekvencije toplotnog zračenja leže u infracrvenom opsegu, tako da ga oko ne percipira (ne vidimo kako „sjajemo“). Kada se tijelo zagrije, njegovi atomi počinju emitovati valove viših frekvencija. Gvozdeni ekser može biti usijan - doveden do takve temperature da će njegovo toplotno zračenje otići u donji (crveni) deo vidljivog opsega. A Sunce nam izgleda žuto-bijelo: temperatura na površini Sunca je toliko visoka da u spektru njegovog zračenja postoje sve frekvencije vidljive svjetlosti, pa čak i ultraljubičaste, zahvaljujući kojima se sunčamo.
Pogledajmo još jednom tri tipa prenosa toplote (slika 3) (slike sa beodom.com).

Rice. 3. Tri vrste prenosa toplote: provodljivost, konvekcija i zračenje
Termodinamika se kao disciplina oblikovala sredinom 19. stoljeća. To se dogodilo nakon otkrića zakona održanja energije. Postoji definitivna veza između termodinamike i molekularne kinetike. Koje je mjesto unutrašnje energije u teoriji? Razmotrimo to u članku.
Statistička mehanika i termodinamika
Originalna naučna teorija termičkih procesa nije bila molekularno-kinetička. Prva je bila termodinamika. Nastala je u procesu studiranja optimalni uslovi korištenje topline za izvođenje radova. To se dogodilo sredinom 19. vijeka, prije nego što je prihvaćena molekularna kinetika. Danas se i termodinamika i molekularno-kinetička teorija koriste u tehnologiji i nauci. Ovo posljednje se u teorijskoj fizici naziva statistička mehanika. Ona, zajedno s termodinamikom, istražuje korištenje razne metode iste pojave. Ove dvije teorije se nadopunjuju. Osnovu termodinamike čine njena dva zakona. Oba se tiču ponašanja energije i uspostavljena su empirijski. Ovi zakoni važe za bilo koju supstancu, bez obzira na unutrašnja struktura. Statistička mehanika se smatra dubljom i preciznijom naukom. U poređenju sa termodinamikom, ona je složenija. Koristi se kada termodinamički odnosi nisu dovoljni da objasne fenomen koji se proučava.

Teorija molekularne kinetike
Sredinom 19. vijeka dokazano je da, uz mehaničku, postoji i unutrašnja energija makroskopskih tijela. Uključen je u bilans energetskih prirodnih transformacija. Nakon što je otkrivena unutrašnja energija, formulisan je stav o njenom očuvanju i transformaciji. Dok pak klizi po ledu prestaje pod uticajem trenja, njegova kinetička (mehanička) energija ne samo da prestaje da postoji, već se prenosi na molekule paka i leda. Prilikom kretanja, hrapavost površina tijela koja su podvrgnuta trenju se deformiraju. Istovremeno se povećava intenzitet nasumično pokretnih molekula. Kada se oba tijela zagriju, unutrašnja energija se povećava. Takođe je lako uočiti obrnuti prelaz. Kada se voda zagrije u zatvorenoj epruveti, unutrašnja energija (i ona i rezultirajuća para) počinje da raste. Pritisak će se povećati, uzrokujući istiskivanje utikača. Unutrašnja energija pare će uzrokovati povećanje kinetičke energije. U procesu ekspanzije, para radi. Istovremeno, njegova unutrašnja energija se smanjuje. Kao rezultat, para se hladi.

Unutrašnja energija. opće informacije
U nasumičnom kretanju svih molekula, zbir njihovih kinetičkih energija, kao i potencijalnih energija njihovih interakcija, je unutrašnja energija. S obzirom na položaj molekula u odnosu jedan prema drugom i njihovo kretanje, gotovo je nemoguće izračunati ovaj zbir. Ovo je zbog veliki iznos elemenata u makroskopskim tijelima. S tim u vezi, potrebno je moći izračunati vrijednost u skladu sa makroskopskim parametrima koji se mogu mjeriti.
Monatomski gas
Tvar se smatra prilično jednostavnom u svojim svojstvima, jer se sastoji od pojedinačnih atoma, a ne molekula. Monatomski gasovi uključuju argon, helijum i neon. Potencijalna energija u ovom slučaju jednaka je nuli. To je zbog činjenice da molekuli u idealnom plinu ne komuniciraju jedni s drugima. Kinetička energija slučajnog molekularnog kretanja je odlučujući faktor za unutrašnje (U). Da bismo izračunali U jednoatomnog plina mase m, trebamo pomnožiti kinetičku energiju (prosjek) 1. atoma sa ukupnim brojem svih atoma. Ali treba uzeti u obzir da je kNA=R. Na osnovu podataka koje imamo, dobijamo sledeću formulu: U= 2/3 x m/M x RT, gdje je unutrašnja energija direktno proporcionalna apsolutnoj temperaturi. Sve promjene u U određuju samo T (temperatura) mjerena u početnom i konačnom stanju gasa i nisu direktno povezane sa zapreminom. To je zbog činjenice da su interakcije njegove potencijalne energije jednake 0 i uopće ne ovise o drugim sistemskim parametrima makroskopskih objekata. U prisustvu složenijih molekula, idealan gas će takođe imati unutrašnju energiju direktno proporcionalnu apsolutnoj temperaturi. Ali, moram reći, u ovom slučaju, između U i T, koeficijent proporcionalnosti će se promijeniti. Uostalom, složeni molekuli izvode ne samo translacijske pokrete, već i rotacijske. Unutrašnja energija jednaka je zbiru ovih kretanja molekula.
Od čega U zavisi?
Na unutrašnju energiju utiče jedan od makroskopskih parametara. Ovo je temperatura. Za stvarne gasove, tečnosti i čvrste materije, potencijalna energija (prosek) tokom interakcije molekula nije jednaka nuli. Mada, ako točnije razmotrimo, za gasove je to mnogo manje od kinetičkog (prosečnog). Istovremeno je za čvrsta i tečna tijela uporediv s njim. Ali prosječno U ovisi o V supstance, jer se tokom perioda njene promjene mijenja i prosječna udaljenost koja postoji između molekula. Iz ovoga sledi da u termodinamici unutrašnja energija zavisi ne samo od temperature T, već i od V (volumena). Njihova vrijednost jednoznačno određuje stanje tijela, pa stoga i U.

Svjetski ocean
Teško je zamisliti kakve nevjerovatno velike rezerve energije sadrže okeani. Razmislite koja je unutrašnja energija vode. Treba napomenuti da je i termalni, jer je nastao kao rezultat pregrijavanja tečnog dijela površine oceana. Dakle, imajući razliku, na primjer, od 20 stepeni u odnosu na dno vode, dobija vrijednost od oko 10 ^ 26 J. Prilikom mjerenja strujanja u okeanu, njegova kinetička energija se procjenjuje na oko 10 ^ 18 J.
Globalni problemi
Postoje globalni problemi koji se mogu staviti na svjetski nivo. To uključuje:
Iscrpljivanje rezervi fosilnih goriva (prvenstveno nafte i gasa);
Značajno zagađenje životne sredine povezano sa upotrebom ovih minerala;
Termičko "zagađenje", plus povećanje koncentracije atmosferskog ugljičnog dioksida, prijeteći globalnim klimatskim poremećajima;
Korištenje rezervi uranijuma, što dovodi do pojave radioaktivnog otpada, koji ima vrlo negativan utjecaj na život svih živih bića;
Upotreba termonuklearne energije.

Zaključak
Sva ta neizvjesnost oko posljedica koje će zasigurno doći ako ne prestanemo da trošimo energiju koja se tako izvlači, tjera naučnike i inženjere da gotovo svu svoju pažnju posvete rješavanju ovog problema. Njihov glavni zadatak je pronalaženje optimalnog izvora energije, a takođe je važno uključiti različite prirodne procese. Među njima su najzanimljiviji: sunce, odnosno sunčeva toplota, vetar i energija u okeanima.

U mnogim zemljama, mora i okeani se dugo smatraju izvorima energije, a njihovi izgledi postaju sve obećavajući. Okean je prepun mnogih tajni, njegova unutrašnja energija je izvor bez dna. Koliko nam načina pruža ekstrakciju energije (kao što su oceanske struje, energija plime, toplinska energija i drugi) već nas tjera da razmišljamo o njegovoj veličini.